Все изменилось, когда шотландец Александр Флеминг приблизился к открытию пенициллина, он сумел облечь свое исследование в научную структурированную форму. Открытие произошло случайно, благодаря неряшливости Флеминга. Он терпеть не мог убирать за собой. Вернувшись из отпуска к работе 3 сентября 1928 года, Флеминг обнаружил, что на одном из планшетов со стафилококками завелась плесень. Культуры стафилококков исчезли, при этом все колонии плесени чувствовали себя совершенно нормально.
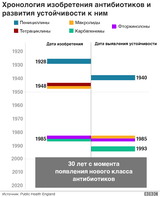
Эти грибы он отнёс к роду пеницилловых и назвал выделенное вещество пенициллином. Это вещество смогло лечить пневмонию, менингиты, гангрены, сифилис, гонорею и другие смертельные заболевания. Но, получить пенициллин в чистом виде получилось лишь в 1940 году, спустя 12 лет после открытия, кгда за дело взялись химики из США Эрнст Чейн и Говард Флори. Первый выделил пенициллин в чистом виде, второй проводил опыты на животных. Впервые в 1942 г препарат ввели человеку, умирающему от менингита. После полученного терапевтического эффекта, пенициллин пустили в массовое производство. Благодаря первому антибиотику удалось спасти много жизней. В 1945-м Флеминг, Флори и Чейн удостоились Нобелевской премии в области физиологии и медицины. Большинство современных антибиотиков были созданы именно после исследования лечебных свойств пенициллина.
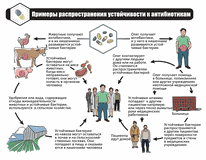
Итак, антибиотики используются в борьбе против бактерий - возбудителей инфекционных заболеваний, а у этих микроорганизмов очень высокая способность приспосабливаться к условиям окружающей среды. Благодаря естественному отбору следующее поколение бактерий получает лучшие качества родительских клеток. У микроорганизмов это получается гораздо лучше, чем у людей, так как новое потомство у бактерий появляется каждые 20–30 минут, а у людей — примерно каждые 20 - 25 лет. В результате высокой адаптивной способности у микроорганизмов формируется устойчивость к препаратам, которыми с ними боролись – антибиотикорезистентность. В настоящее время, имеется более пятнадцати групп разнообразных антибактериальных препаратов, причем не только с антибактериальным, но и противогрибковым, противоопухолевым действием. Однако, рациональный выбор препарата сделать всё труднее, а это связано с ростом устойчивости бактерий. Если раньше у возбудителя болезни вырабатывалась устойчивость к какому-то одному антибиотику, использовали комбинации из нескольких, чтобы они уж точно уничтожили патоген. Сегодня появились бактерии, резистентные сразу к нескольким химически несхожим антибиотикам, что во много раз обострило ситуацию. По оценкам ученых, в 2019г. устойчивость бактериальных инфекций к противомикробным препаратам стала причиной смерти 1,27 миллиона человек. Антибиотикорезистентность приводит к тому, что болезнь продолжает прогрессировать, переходит в более тяжелую форму. Особо опасно, когда поражаются жизненно важные органы: сердце, легкие, головной мозг и т.д. Ряд заболеваний приобретает хроническое течение и человек становится носителем резистентных штаммов, источником инфекции. Заболевания, вызываемые такими штаммами, характеризуются более длительным, тяжелым течением, чаще требуют госпитализации, ухудшают прогноз, увеличивают стоимость лечения.
Сегодня ВОЗ называет сегодня устойчивость к антибиотикам одной из главных опасностей для глобального здравоохранения. Например, всё труднее становится лечить пневмонию, туберкулёз, гонорею и сальмонеллёз. Ожидается, что к 2050 году супербактерии убьют людей больше, чем рак, — 10 млн человек. Сейчас из-за устойчивости к антибиотикам ежегодно умирает 700 тысяч человек.